






Механизму развития болезни Альцгеймера посвящено несколько гипотез. Одной из наиболее распространенных и общепринятых считается так называемая амилоидная гипотеза.
Амилоиды — а точнее, бета-амилоидные пептиды — представляют собой молекулярную конструкцию белкового типа и в нормальном, здоровом своем состоянии заняты защитой нервных клеток мозга. Срок им определен короткий, и, выполнив свою функцию, они попадают под «ножи» протеаз, белков-чистильщиков, изрезающих на мелкие кусочки все, ставшее ненужным, и превращающих амилоиды в безопасные "шлаки", которые затем утилизируются или выводятся из организма. Но, согласно гипотезе, иногда наступает момент, когда что-то идет не так, и защитники нервных клеток превращаются в их убийц. Более того, эти пептиды начинают объединяться между собой с образованием агрегатов и становятся недоступны для «ножей» протеаз. Более или менее детально этот механизм в рамках амилоидной гипотезы прописан на этапах, присущих болезни уже в развитой стадии, когда появляются токсичные агрегаты, и далее, когда мозг уже покрывается амилоидными бляшками. О начальной же стадии процесса превращения бета-амилоида в опасные для нервных клеток продукты было известно очень мало.
«Было, например, известно, — говорит один из авторов статьи Владимир Польшаков, — что важную роль в инициализации этих процессов играют ионы переходных металлов, прежде всего цинка. Цинк, вообще говоря, выполняет в мозге массу полезных и важных функций, однако здесь он был на очень серьезных основаниях заподозрен во "вредительстве", в том, что именно он является одним из инициализаторов каскада процессов, приводящих к болезни Альцгеймера. Однако что конкретно происходит при взаимодействии молекул бета-амилоидного пептида с ионами цинка, с какими аминокислотными остатками связываются эти ионы, и как такое связывание стимулирует процессы агрегации пептида, оставалось неясным. Мы поставили перед собой задачу прояснить хотя бы часть этих вопросов».
Ученые исследовали различные патогенные бета-амилоидные пептиды, а точнее, их короткие участки, домены, связывающие их с металлами. В работе применялись различные методы, основным из которых была спектроскопия ядерного магнитного резонанса (ЯМР), с ее помощью определялись структуры образующихся молекулярных комплексов. Некоторые спектры, требующие повышенной чувствительности прибора, были дополнительно измерены в Великобритании. В выборе патогенов, по словам Польшакова, исследователям "частично повезло". Одним из патогенов был так называемый "английский мутант", отличающийся от нормального бета-амилоидного пептида всего лишь одной аминокислотной заменой. С помощью ЯМР ученым удалось детально разобраться с протекающими химическими процессами и изменениями структуры в ходе связывания пептида с ионами цинка и дальнейшей агрегации.
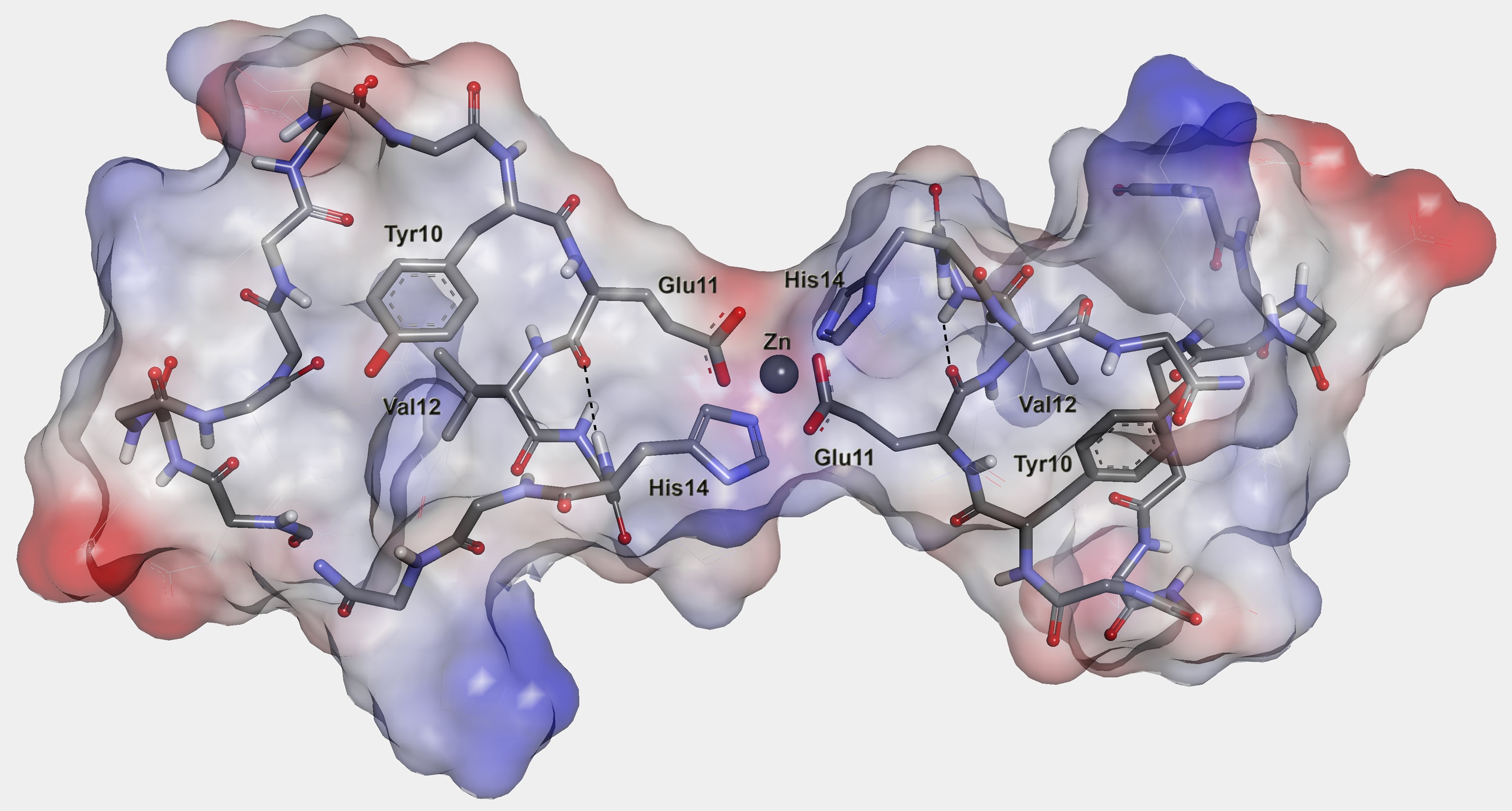
Вторым изученным патогеном был изомеризованный бета-амилоидный пептид. Он по химическому составу не отличается от нормального пептида человека, но один из его аминокислотных остатков, аспарагиновая кислота, представляет собой молекулу с другим взаимным расположением атомов. Такая изомеризация протекает спонтанно, без участия ферментов, и поэтому связана с процессом старения — еще одного важного фактора развития болезни Альцгеймера. Коллеги из Института молекулярной биологии РАН недавно показали, что введение изомеризованного пептида трансгенным мышам быстро приводит к образованию у них амилоидных бляшек. В присутствии ионов цинка металлсвязывающий домен этого пептида агрегировал столь быстро, что образующиеся структуры просто не успевали детектировать. Однако ученым удалось выяснить, что, несмотря на все различия в процессах, протекающих с "английским мутантом" и изомеризованным пептидом, начальные стадии у них оказались совершенно одинаковыми. В обоих случаях спусковой крючок оказался одним и тем же — роль зародышей патогенной агрегации в обоих случаях играли образующиеся в самом начале патогенные димеры пептида, т.е. две молекулы пептида, скрепленные ионом цинка. Такие же димеры наблюдались и в случае нормального пептида человека, а различия для всех исследованных форм были связаны со скоростью образования димеров и их склонностью к дальнейшей агрегации.
Основываясь на этом сходстве, исследователи разработали предполагаемый механизм контролируемой ионами цинка процедуры превращения пептида-защитника в пептид-убийцу. Этот механизм, отмечают ученые, объясняет многие экспериментальные факты, полученные не только ими, но и их коллегами в других лабораториях, изучающих болезнь Альцгеймера. Ученые также надеются, что их открытие за счет точного выбора мишени поможет создавать новые лекарства, способные блокировать инициализируемую ионами цинка агрегацию бета-амилоидных пептидов.

