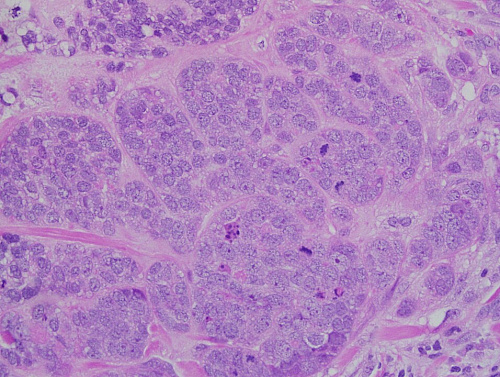
Многообещающий подход для комбинированной тераностики рака (комбинации диагностики и терапии при использовании одного соединения) — комбинация иммунотерапии и направленной доставки химиотерапевтических соединений, например, с использованием наночастиц. Однако этот подход сегодня демонстрирует лишь ограниченный успех в связи с рядом проблем, таких как низкий терапевтический индекс традиционной химиотерапии, отсутствие широкого спектра онкомаркеров на поверхности клеток и других факторов.
«Мы разработали стратегию синергичной комбинированной адресной иммуно/химиотерапии: мы нацеливаем препараты на разные участки одного рецептора — онкомаркера HER2 на поверхности клеток. HER2 — клинически значимый онкомаркер, повышенное количество которого на поверхности клеток часто ассоциировано с устойчивостью к химиотерапии, высоким метастазированием и плохим прогнозом», — говорит руководитель проекта по гранту РНФ Виктория Шипунова, старший научный сотрудник Лаборатории молекулярной иммунологии ИБХ РАН.
Ученые нацелили на опухоль сразу два компонента. Во-первых, наночастицы полилактида-когликолида — сополимера молочной и гликолевой кислот, то есть композита из веществ, которые есть в организме человека. Шарики-наночастицы «заправили» химиопрепаратом доксорубицином, а также адресным полипептидом — аффибоди, который распознает молекулы HER2 на поверхности раковых клеток, и красителем, позволяющим увидеть, что происходит в организме после запуска препарата.
В качестве второго компонента использовали фрагмент токсина из синегнойной палочки, связанного с другим адресным полипептидом, узнающим онкомаркер HER2. Этот полипептид — дарпин9.29 — связывает другой участок рецептора HER2, не конкурируя за место связывания с аффибоди.
В своей работе ученые впервые использовали адресные скаффолдовые полипептиды, чтобы нацелиться на один онкомаркер — HER2. Скаффолдовые полипептиды — новый популярный класс нацеливающих соединений, который используют вместо традиционных полноразмерных антител. Они меньше, реже вызывают нежелательный ответ иммунитета, хорошо растворимы и стабильны в экстремальных условиях, а также гораздо легче и дешевле синтезируются в биореакторах, что немаловажно для их дальнейшего массового применения в биомедицине.
«Использование двух адресных суперструктур позволило в 1000 раз снизить концентрацию действующих веществ для достижения того же терапевтического эффекта. Более того, комбинация этих препаратов действует синергично, то есть одно вещество значительно усиливает действие другого. Это особенно удивительно и неожиданно, поскольку оба препарата воздействуют всего на один клеточный рецептор. Такая синергия позволила значительно усилить эффективность терапии HER2-позитивных опухолей у животных и полностью предотвратить появление метастазов», — рассказывает Виктория Шипунова.
В работе ученые для тестирования своих разработок использовали иммунодефицитных мышей, у которых нет тимуса, что приводит к низкому количеству защитных клеток организма — T-лимфоцитов. Таким мышам подсаживали человеческие раковые клетки, несущие на себе человеческий онкомаркер HER2, и отсутствие достаточных защитных сил иммунитета мышей позволило этим клеткам «прижиться» в мышином организме и сформировать метастазирующую опухоль. Соответственно, исследователи получили удобную модель для доклинических исследований злокачественного роста — у мышей формировались опухоли, напоминающие человеческие и реагирующие на лечение так же, как реагировали бы человеческие раковые клетки.
Поскольку разработанные препараты — разные по происхождению и значению, они выводятся из организма разными путями: наночастицы — через печень или селезенку, белки — через почки. Таким образом, комбинируя лечебные средства и снижая их концентрацию, можно добиться минимизации воздействия на органы («перераспределив» общую сильную нагрузку, например, на печень, между всеми органами в гораздо меньшей дозе) и кардинального уменьшения побочных эффектов, что очень важно для разработки эффективных стратегий онкотераностики.
«Разработанная стратегия двойного нацеливания, подразумевающая "два агента — один рецептор" — большой шаг на пути к разработке эффективных методов лечения агрессивных опухолей. Эту стратегию можно распространить на другие комбинированные методы лечения и противоопухолевые мишени», — полагает Сергей Деев, доктор биологических наук, профессор, академик РАН, руководитель исследования, заведующий лабораторией молекулярной иммунологии, где была выполнена основная часть работы.