Криохирургия — один из методов удаления различных злокачественных новообразований, таких как рак молочной железы, легких, печени и почек. Пораженную ткань точечно замораживают непосредственно в теле человека, что вызывает гибель злокачественных клеток. Главные достоинства криохирургии заключаются в том, что это — высокоэффективный тип вмешательства, который не требует иссечения опухоли и не вызывает побочных эффектов, неизбежных, например, при химиотерапии рака.
Ткань, которую удаляют методом криохирургии, необходимо очень быстро охладить до температуры от -20°C до -40°C, чтобы злокачественные клетки разрушились из-за образующихся в них кристаллов льда. Гибели этих клеток также способствуют обезвоживание и нарушение поступления кислорода из-за низких температур. Для этого специалисты используют криозонды — металлические устройства для контакта с тканями человека, предварительно охлаждаемые различными способами (например, с помощью жидкого азота). Чтобы заморозка не повредила здоровые клетки, прилегающие к новообразованию, весь процесс отслеживают с помощью ультразвукового исследования (УЗИ), магнитно-резонансной томографии (МРТ) или компьютерной томографии (КТ). Однако эти подходы имеют свои недостатки: для проведения УЗИ при криохирургических операциях нужен специальный датчик, а МРТ и КТ до сих пор остаются достаточно дорогими методами.
Ученые из
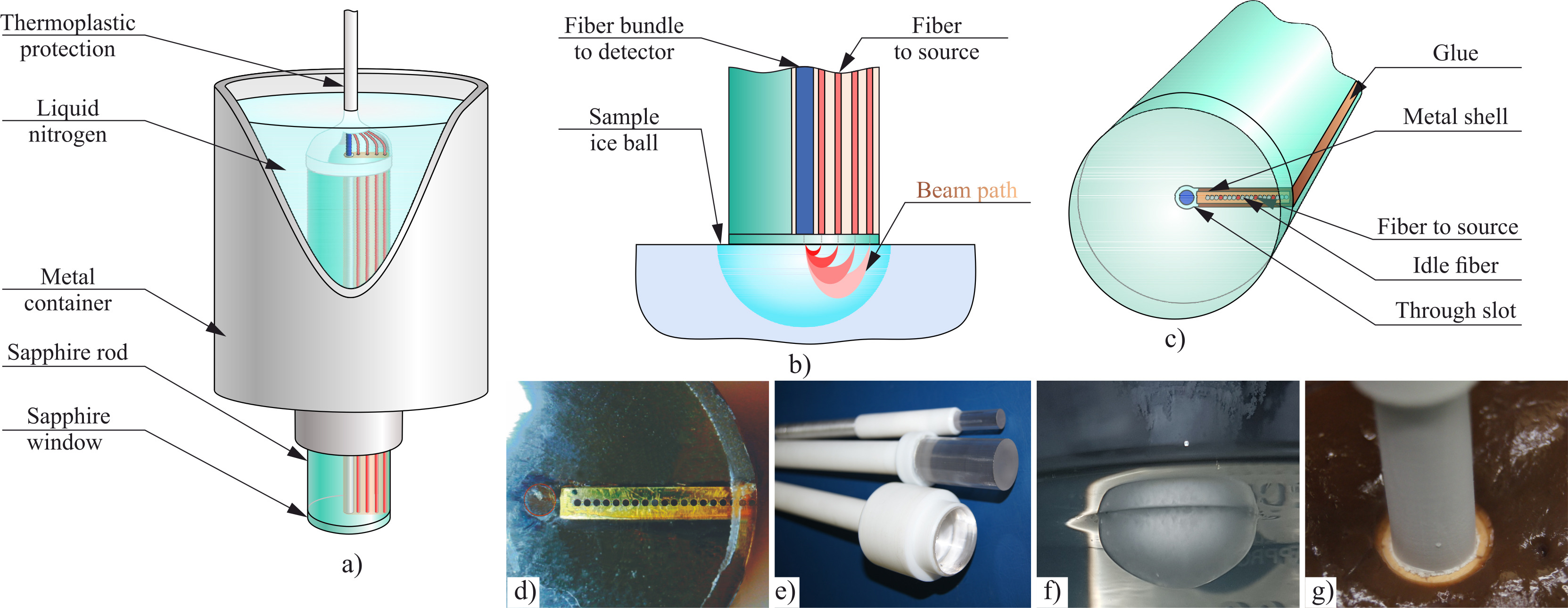
Института физики твердого тела имени Ю. А. Осипьяна РАН (Черноголовка) в сотрудничестве с российскими коллегами разработали сапфировый криозонд, с помощью которого можно не только замораживать ткань в ходе операции, но и наблюдать за процессом охлаждения. Чтобы устройство выполняло обе эти задачи, авторы вырастили кристалл сапфира, внутри которого в специальных каналах поместили оптические волокна. Они соединены с источником излучения и детектором, который регистрирует диффузно отраженный от освещаемой в разных точках ткани свет. Таким образом, когда криозонд охлаждает клетки, он одновременно подсвечивает их лазером и улавливает отраженное излучение. По этому излучению можно определить, какой объем ткани оказался замороженным в каждый момент времени.
Исследователи экспериментально проверили устройство, заморозив искусственный образец, имитирующий по оптическим свойствам живую ткань. Наблюдая при этом за интенсивностью отраженного света, ученые получили математическую модель, описывающую весь процесс замораживания ткани криозондом. Это позволило настроить устройство и подготовить его к использованию на реальных человеческих тканях.
«Криозонд можно легко адаптировать для операций различного масштаба, поскольку размер рабочей площади устройства, которая осуществляет заморозку, может варьироваться от нескольких миллиметров до нескольких сантиметров. Наши эксперименты показали, что криозонд позволяет с точностью до двух миллиметров оценивать состояние ткани в образцах толщиной до десяти миллиметров. В дальнейшем мы продолжим работу, чтобы улучшить его возможности», — рассказывает руководитель проекта, поддержанного грантом РНФ, Ирина Долганова, кандидат технических наук, старший научный сотрудник лаборатории профилированных кристаллов Института физики твердого тела имени Ю. А. Осипьяна РАН.
В работе также принимали участие исследователи из
Московского государственного технического университета имени Н. Э. Баумана (Москва),
Института общей физики имени А. М. Прохорова РАН (Москва), Сеченовского университета (Москва) и
Саратовского государственного университета (Саратов).
Если вы хотите стать героем публикации и рассказать о своем исследовании, заполните форму на сайте РНФ