







Ученые из Казанского (Приволжского) федерального университета с коллегами исследовали, как противомалярийный препарат мефлохин влияет на работу клеточных структур в организме, отвечающих за сборку белка. Как пояснили специалисты, ДНК — это молекула, хранящая информацию о структуре всех белков в организме. А при синтезе определенного белка в клетке с фрагмента ДНК копируется молекула РНК. Образовавшуюся последовательность нуклеотидов считывает рибосома.
Чтобы рибосома не останавливалась и продолжала правильный синтез белка, потенциально можно использовать антибиотики аминогликозиды. Авторы исследования впервые определили, как меняется структура рибосом в клетках грибов в присутствии противомалярийного препарата мефлохина этих веществ. Для этого исследователи использовали криоэлектронную микроскопию — вариант электронной микроскопии, при котором образцы изучаются при низких температурах, — а также рентгеновскую кристаллографию. Это метод, который позволяет установить трехмерную структуру соединений по тому, как их кристаллы рассеивают рентгеновские лучи.
Оказалось, что мефлохин вызывает поворот фрагментов рибосомы относительно друг друга, тем самым усиливая действие аминогликозидов, что позволяет структуре продолжить синтез белка.
— Мы разработали новый метод кристаллизации рибосом дрожжеподобных грибов Candida albicans, который позволяет увидеть малые молекулы в активных центрах рибосомы, что ранее было трудно осуществить методом криоэлектронной микроскопии. Добавив к ней данные рентгеновской кристаллографии, мы смогли увидеть в 3D с атомарным разрешением, как меняется структура рибосомы при связывании с различными молекулами. Мы с коллегами продолжаем изучать структуры рибосом из различных организмов, чтобы более полно понимать основы протекания биохимических процессов внутри клетки, — рассказал «Известиям» участник проекта, доктор физико-математических наук, профессор кафедры медицинской физики КФУ Константин Усачев.
Полученные данные позволят разработать лекарственные препараты, взаимодействующие с рибосомами и запускающие дальнейший синтез белка в клетках пациентов, которые страдают от наследственных заболеваний, связанных с нарушением синтеза белка.
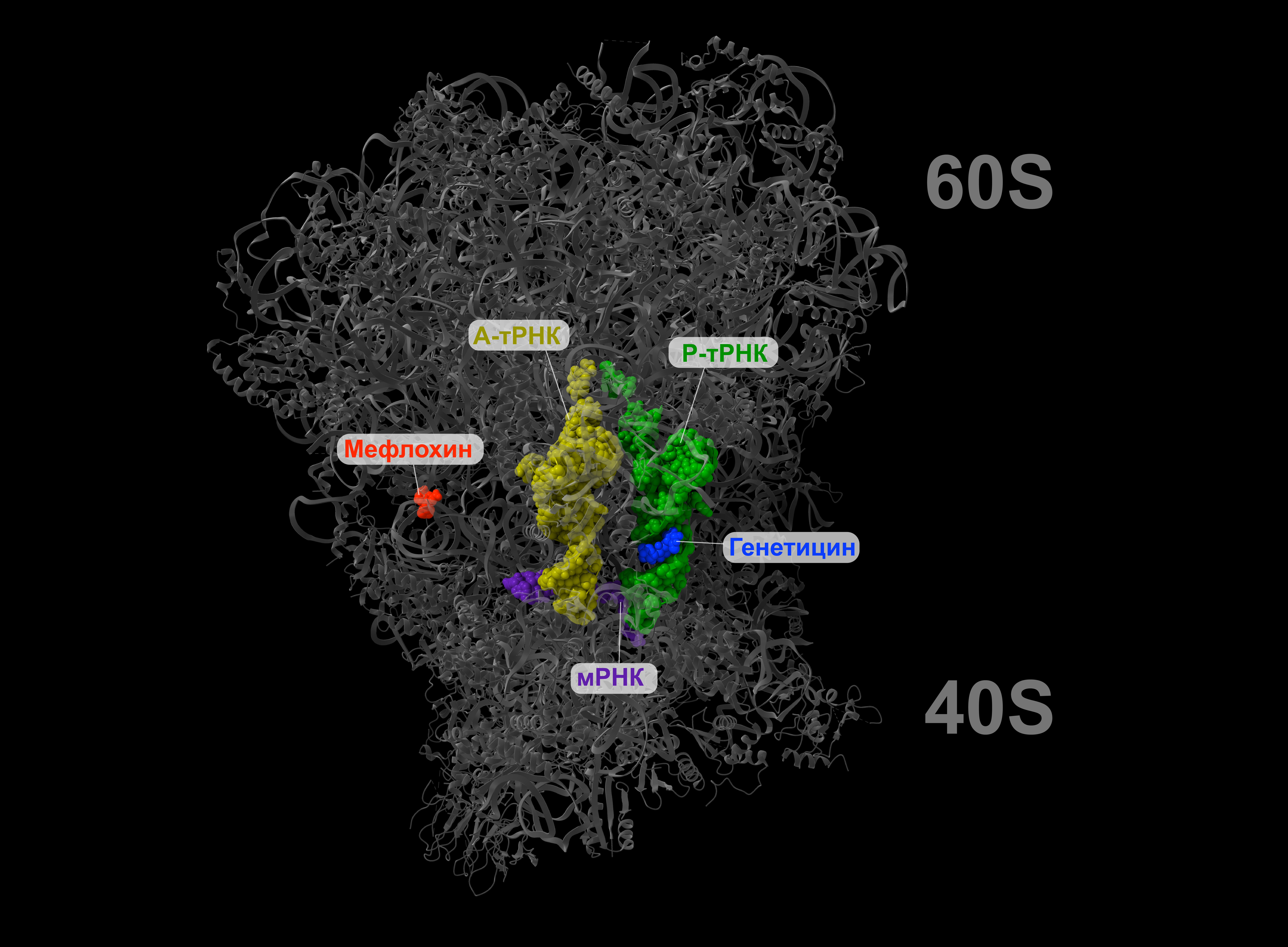
Трехмерная структура рибосомы. Источник: Константин Усачев
Наш организм работает благодаря белкам — именно они выполняют почти все функции в клетках. Но, чтобы создать белок, клетке нужно прочитать «рецепт» из ДНК и собрать молекулу по инструкции. Этим занимается специальная клеточная машинка — рибосома. Она, словно сборочный конвейер, считывает код и собирает из аминокислот сложные белковые структуры. Без этой работы не было бы ни мышц, ни кожи, ни гормонов, пояснил «Известиям» эксперт НТИ «Хелснет», ученый-биолог, основатель биомедтех-стартапов BioAlg Corp. и OncoUnite Дмитрий Чебанов.
— Ученые обнаружили: если добавить к аминогликозидным антибиотикам противомалярийный препарат мефлохин, рибосома может «перешагнуть» через эту ошибку и продолжить сборку. То есть буквально проигнорировать ложный сигнал «стоп» и достроить полноценный белок. Это похоже на ситуацию, когда на производстве бракованная инструкция велит прекратить работу, но опытный мастер понимает, что это ошибка, и достраивает изделие до конца. Ранее для такого эффекта требовались большие дозы антибиотиков, что вредно для организма, — отметил ученый.
Исследование открывает новый путь — лечить генетические болезни не редактированием ДНК, а более мягким вмешательством, влияя на то, как клетка «читает» уже имеющийся код. Это дешевле, проще и потенциально безопаснее, подчеркнул Дмитрий Чебанов.
Исследование дает надежду на разработку нового подхода к лечению МДД и других наследственных заболеваний, обусловленных преждевременными стоп-кодонами, рассказала «Известиям» врач-генетик, научный сотрудник отдела орфанных болезней и профилактики инвалидизирующих заболеваний НИИ педиатрии и охраны здоровья детей НКЦ № 2 ФГБНУ «РНЦХ им. академика Б.В. Петровского» Вероника Попова.
— Пока оно проведено на клетках грибов, но если аналогичный эффект подтвердится на человеческих клетках, это откроет путь к клиническим испытаниям. Потребуются дополнительные исследования на животных моделях МДД (например, мышах с мутацией в гене дистрофина). Если дальнейшие испытания подтвердят эффективность и безопасность комбинации мефлохина и аминогликозидов, это может стать новым вариантом терапии не только МДД, но и других болезней, вызванных нонсенс-мутациями. Однако на разработку и внедрение такого препарата потребуется не менее 5–10 лет, — рассказала специалист.
Мышечная дистрофия Дюшенна — врожденное, неуклонно прогрессирующее генетическое заболевание, приводящее к потере способности ходить к 10–12 годам и заканчивающееся смертью от сердечно-легочной недостаточности на третьем десятилетии.
Результаты исследования, поддержанного несколькими грантами Российского научного фонда (РНФ), опубликованы в журнале Proceedings of the National Academy of Sciences (ред. - Пресс-служба РНФ).— В России диагностировано около 1,3 тыс. детей с МДД. Сегодня в мире есть препараты, способные изменить траекторию заболевания и значительно улучшить качество и продолжительность жизни пациентов. Эта терапия подходит пациентам с определенными мутациями, — отметили в пресс-службе «Р-Фарм».
Если вы хотите стать героем публикации и рассказать о своем исследовании, заполните форму на сайте РНФ.

